Последние конференции
- Информационные системы и модели в научных исследованиях, промышленности, образовании и экологии
- Информационные системы и модели в научных исследованиях, промышленности и экологии
- Современные проблемы экологии
- Экологические проблемы окружающей среды, пути и методы их решения
- Экология, образование и здоровый образ жизни
Моделирование биокоррозии металлов
М.В. Челнокова, Д.В. Белов, Т.Н. Соколова, О.В. Кузина, В.Р. Карташов
Нижегородский государственный технический университет им. Р.Е. Алексеева,
г. Н. Новгород
Известно, что в естественных условиях, под воздействием микроорганизмов, металлы подвергаются коррозионному разрушению, которое часто рассматривают как биологическую коррозию. В настоящей работе были смоделированы условия разрушения металлов при участии микроорганизмов, широко представленных в природе (почве, воздухе, воде), в оптимальном режиме их жизнедеятельности.
В качестве объектов исследований использовались металлы Al и его сплавы (В65, Д16, Д16Т и АД0), а также Mg, Zn, Cd, Bi, Sn, Pb. Были выявлены наиболее активные микроорганизмы, в числе которых микромицеты Aspergillus niger, Aspergillus orizae, Alternaria alternata и бактерииStaphylococcusaureus, Proteusvulgaris, Pseudomonasaeruginosa. Установлено, что в не зависимости от природы поверхности металла микромицетная коррозия протекает через ряд последовательных этапов: образование на всех поверхностях металлов жидкого экссудата с pH>7, в виде локальных, прозрачных, легко подвижных капель, который через ряд стадий, включая гелеобразование, превращался в продукты коррозии оксидной природы. Характер изменений поверхности металлов позволил сделать предположение, что определяющую роль на начальной стадии могу играть активные формы кислорода (АФК), продуцируемые микроорганизмами [1 – 3].
Возможность участия АФК подтверждена с использованием модельных систем, с адсорбцией на поверхности металлов соединений, способных к специфическому взаимодействию с O2–• и другими АФК. Адсорбция на поверхности алюминия ионола и гидрохинона способствовала усилению коррозии (рис. 1). АФК зафиксированы при использовании хлорида тетразолия нитросинего.
Анализ состава образований на поверхности металла на заключительных этапах микромицетной коррозии спустя 40-60 суток экспозиции, показал наличие ряда органических кислот – продуктов метаболизма, таких как пировиноградная, лимонная, α-кетоглутаровая, янтарная, фумаровая, яблочная, миристиновая, пальмитиновая, олеиновая, стеариновая, линолевая. В случае воздействия бактерий в преобладающем количестве обнаружены аминокислоты и аммиак. Для выяснения роли микроорганизмов на заключительных этапах были смоделированы условия воздействия кислот и их смесей на поверхность металлов, из числа обнаруженных при биокоррозии. В качестве примера приведена гистограмма коррозионных повреждений образцов сплава Д16 (рис. 1). Как видно из рисунка, характер разрушений при воздействии микроорганизмов более заметный, чем при действии на металл модельных систем. По-видимому, вещества, обладающие сами по себе умеренной или слабой коррозионной активностью, в составе сложного метаболита, включающего помимо идентифицированных соединений и другие продукты жизнедеятельности, например ферменты, прежде всего класса оксидоредуктаз, пероксид водорода, проявляют себя как более сильные биодеструкторы. В связи с чем, моделирование процессов, протекающих с участием биологических объектов и адекватно отражающих физико-химические закономерности, на наш взгляд, нельзя осуществлять в отсутствие микроорганизмов. Оценку проводили с помощью бальной системы [1 – 3].
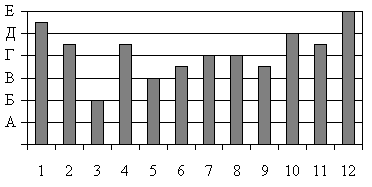
Рис. 1. Гистограмма коррозионных повреждений образцов сплава Д16 в модельных коррозионных системах на 40-е сутки экспозиции: 1 – степень повреждения образца микроскопическим грибом Aspergillusniger; 2 – бактерией Pseudomonasaeruginosa; 3 – смесью аминокислот (Асп, Арг, Вал, Гис, Глу, Лей, Сер, Три, Цис); 4 – смесью аминокислот с добавлением 0,01 М раствора NH3?H2O; 5 – смесью кислот цикла Кребса (пировиноградная, лимонная, α-кетоглутаровая, янтарная, фумаровая, яблочная); 6 – смесью жирных кислот (миристиновая, пальмитиновая, олеиновая, стеариновая, линолевая); 7 – смесью, составленной из систем 3, 5; 8 – смесью, составленной из систем 3, 6; 9 – смесью, составленной из систем 5, 6; 10 – смесью, составленной из систем 5, 6 с добавлением 0,01М раствора Н2О2; 11 – смесью, составленной из систем 3, 5, 6; 12 – степень повреждения образцов, обработанных 0,01М растворами ионола в гексане и гидрохинона в ацетоне.
Примечание: А – появление экссудата в виде прозрачной жидкости; Б – образование матовых пятен в местах скопления экссудата; В – гелеобразование; Г – кристаллизация геля; Д–появление продуктов коррозии; Е–разрушение более 50 % площади поверхности образцов.
Список литературы
1. Смирнов, В.Ф., Белов, Д.В., Соколова, Т.Н., Кузина О.В., Карташов В.Р. Микробиологическая коррозия материалов на основе алюминия // Прикладная биохимия и микробиология. 2008. Т. 44. № 2. С. 213–218.
2. Белов Д.В., Соколова Т.Н., Смирнов В.Ф., Кузина О.В., Косюкова Л.В., Карташов В.Р. Коррозия алюминия и его сплавов под воздействием микроскопических грибов // Коррозия: материалы, защита. 2007. № 9. С. 36-41.
3. Белов Д.В., Смирнов В.Ф., Соколова Т.Н., Кузина О.В., Карташов В.Р. Коррозия алюминия и алюминиевых сплавов под воздействием микроорганизмов // Известия Вузов. Сер. Химия и химическая технология. 2007. Т. 50. № 6. С. 60 – 64.